Moderna的呼吸道合胞病毒mRNA疫苗进入关键性3期临床试验
近日,Moderna公司宣布,数据和安全监测委员会(DSMB)已批准其预防呼吸道合胞病毒(RSV)的候选疫苗mRNA-1345开展关键性3期临床试验。此次DSMB的认可来自于对mRNA-1345的初步2期临床试验数据的独立审评,该审评表明,在选定剂量下,疫苗在老年人中具有可接受的安全性特征。
RSV是一种常见的呼吸道病毒,一般会引起感冒样症状。虽然大多数感染RSV的人大约在一到两周内康复,但这种病毒对幼儿和老年人可能导致严重后果。对于这些高危人群,RSV是导致包括肺炎和呼吸窘迫在内的严重呼吸道疾病的主要原因。
RSV引起的疾病负担是巨大的,在美国,每年大约有177000例65岁及以上的成年人因感染RSV住院,以及约14000例RSV患者死亡,每年的医疗费用近30亿美元。2021年6月,美国疾控中心发布了健康警报,指出美国某些地区的季节性RSV感染增加,全球也出现了类似的趋势。但目前尚未有批准的疫苗来预防RSV。
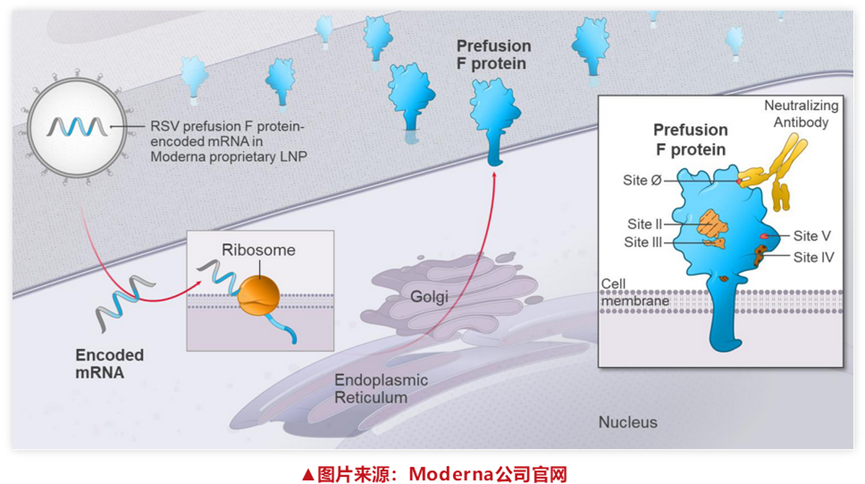
mRNA-1345是一种编码RSV融合前F糖蛋白的疫苗,与融合后状态相比,可引起更高的中和抗体反应。mRNA-1345使用与Moderna的新冠疫苗相同的脂质纳米颗粒(LNP),包含优化的蛋白和密码子序列。此次3期临床试验的主要目标是确定mRNA-1345疫苗在60岁以上成人中的安全性和有效性,从而获得上市许可。
Moderna称此次3期临床试验将在多个国家招募约34000名受试者参与。曾在去年8月3日,FDA就已授予mRNA-1345快速通道资格,用于60岁以上成人任取单剂注射预防RSV感染。
本篇内容来源为第三方转载,本网所有转载文章系出于传递更多信息之目的,且明确注明来源和作者,不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。